研究培育出抗艾滋病毒感染白细胞
来源:PNAS
作者:Yuet Wai Kan
时间:2014-06-23
在战胜艾滋病的漫漫长路上,人类又迈出了一小步。美国加州大学旧金山分校的科学家日前借助基因编辑技术,用诱导多能干细胞(iPS细胞)成功培育出能够对抗艾滋病毒感染的白细胞。除白细胞外,这种iPS细胞还可以被培育成其他类型的血液细胞。研究人员称,该策略有望成为功能性治愈艾滋病的新方法。相关论文发表在美国《国家科学院学报》上。
此前的研究发现,艾滋病病毒往往会通过锁定患者体内CCR5蛋白的方式,对一种名为CD+4 T的细胞展开攻击,破坏人类免疫系统,但这种感染过程在一小部分欧洲人身上的进展却极为缓慢。原因是其体内与CCR5相关的基因发生了突变,产生了一种名为CCR5Δ32的副本。具备这种突变基因的人对艾滋病病毒具有天然的抵抗力。获得这一发现后,科学家们自然会想到,用干细胞移植的方法,将这种突变基因转入艾滋病患者体内,达到治愈艾滋病的目的。
一个众所周知的例子是世界上第一位、也是迄今唯一一位被治愈的艾滋病患者——蒂莫西·雷·布朗。这位48岁的美国人,1995年被检测出感染艾滋病病毒,2006年又被诊断出患急性骨髓性白血病。但之后在两次骨髓干细胞移植手术后,他奇迹般地康复,体内的艾滋病病毒也杳无踪迹。但遗憾的是,布朗的幸运是无法复制的,拥有这种突变基因的人,仅占欧洲人的1%。除了巨额的医疗费用和极大的移植风险外,要找到合适的对艾滋病病毒“免疫”的骨髓配型,完全是一次小概率事件。
新研究的目标就是要在无需CCR5Δ32基因捐献者的情况下,实现同样的效果。美国加州大学旧金山分校华裔遗传学家简悦威(音译)和他的团队借助第三代基因编辑技术CRISPR-Cas9系统,在iPS细胞中插入CCR5Δ32基因片段,而后将其培育成白细胞。与传统基因编辑技术相比,新技术效率更高,在插入位置上也更为精确。物理学家组织网6月11日报道称,目前简悦威的小组已经证明,CRISPR-Cas9系统能够有效地进行基因编辑工作。实验结果证实,他们培育出的具有CCR5Δ32基因片段的白细胞的确能够免受艾滋病病毒的感染。
目前该研究还停留在实验阶段,简悦威的小组还未将这些经过基因编辑的iPS细胞培育成CD+4 T这样特殊类型的白细胞。在细胞类型转换和移植上,还有很多因素需要考虑,距临床应用还有很长的一段路要走。但可以肯定的是,该成果为艾滋病的治疗带来了一种新可能。(来源:科技日报 王小龙)
Seamless modification of wild-type induced pluripotent stem cells to the natural CCR5Δ32 mutation confers resistance to HIV infection
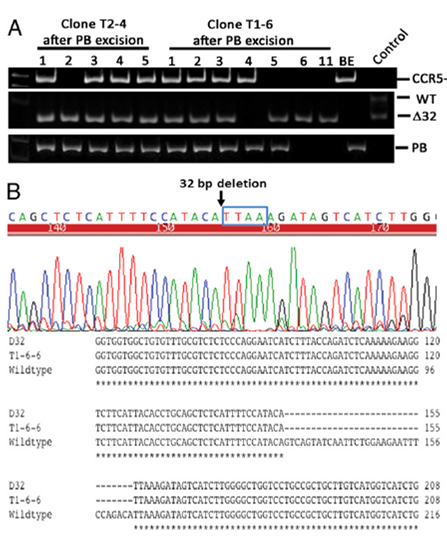
Abstract Individuals homozygous for the C-C chemokine receptor type 5 gene with 32-bp deletions (CCR5Δ32) are resistant to HIV-1 infection. In this study, we generated induced pluripotent stem cells (iPSCs) homozygous for the naturally occurring CCR5Δ32 mutation through genome editing of wild-type iPSCs using a combination of transcription activator-like effector nucleases (TALENs) or RNA-guided clustered regularly interspaced short palindromic repeats (CRISPR)-Cas9 together with the piggyBac technology. Remarkably, TALENs or CRISPR-Cas9–mediated double-strand DNA breaks resulted in up to 100% targeting of the colonies on one allele of which biallelic targeting occurred at an average of 14% with TALENs and 33% with CRISPR. Excision of the piggyBac using transposase seamlessly reproduced exactly the naturally occurring CCR5Δ32 mutation without detectable exogenous sequences. We differentiated these modified iPSCs into monocytes/macrophages and demonstrated their resistance to HIV-1 challenge. We propose that this strategy may provide an approach toward a functional cure of HIV-1 infection.
原文链接:http://www.pnas.org/content/early/2014/06/04/1407473111.full.pdf+html




