成都生物所马小锋团队通过光氧化还原催化攻克糖环双位点选择性C-烷芳基化难题,为糖基药物研发开辟新路径
来源:生物资源利用中心
作者:谢德盟
时间:2025-11-28
糖类物质是药物研发的重要基础,在药物研发领域具有不可替代的地位。从治疗糖尿病的恩格列净 (Empagliflozin),到天然产物沙托霉素B (Saptomycin B),众多临床药物和活性分子均以糖结构为核心骨架。然而,对糖分子进行精准化学修饰一直是个难题。现有方法大多只能在单个位点进行改造,虽有一定成效,却无法匹配临床药物中双位点修饰糖衍生物的结构需求。
近日,中国科学院成都生物研究所马小锋团队巧妙融合光氧化还原催化与自由基Smiles重排策略,开发出一种高效的糖烯1,2-烷芳基化反应,首次实现了糖分子C1和C2位的同步、精准碳基修饰,为构建结构多样的复杂糖衍生物提供了模块化解决方案,有望加速糖基抗肿瘤药物、降糖药物等的研发进程。
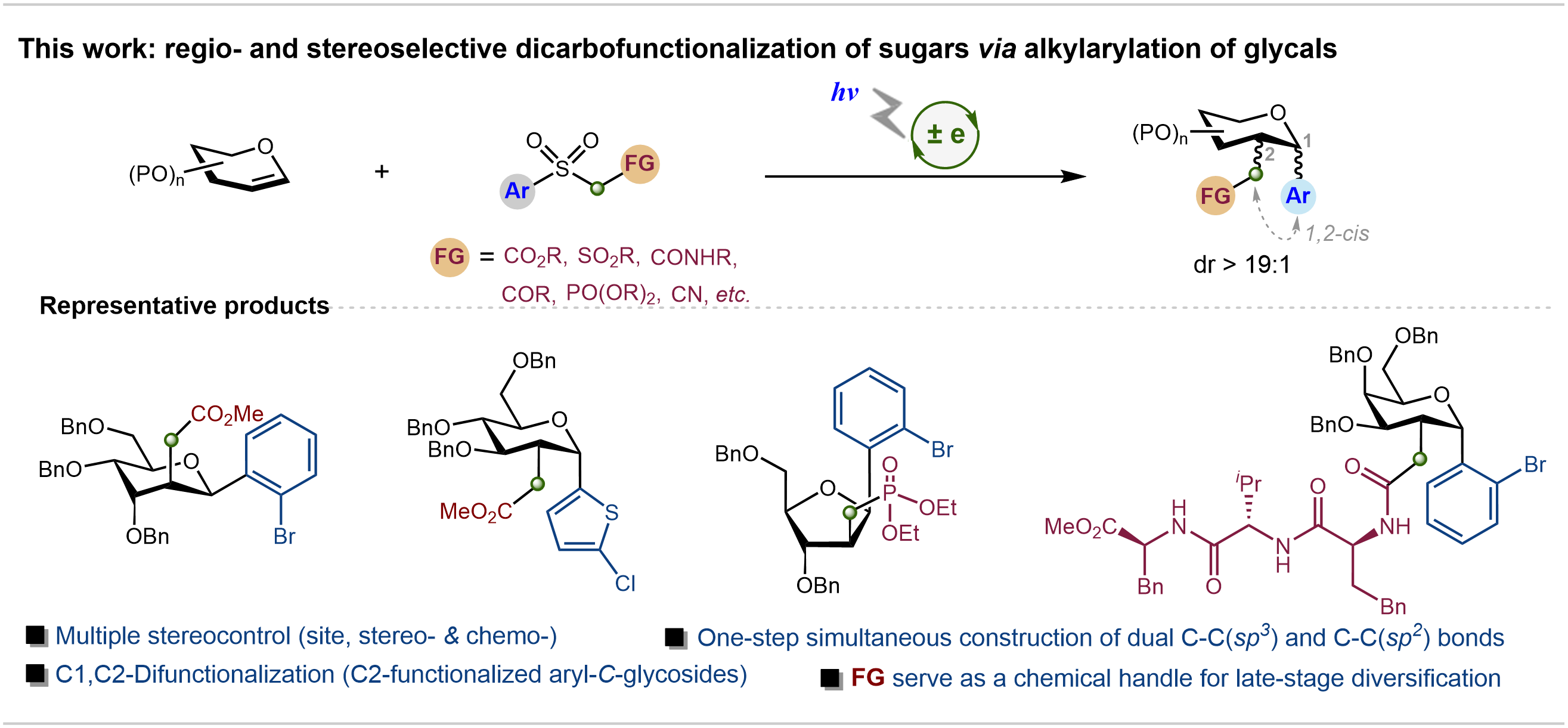
图1. 糖环双位点高区域与立体选择性C-烷芳基化
目前学界对糖分子单一位点(如C-糖基化)的修饰技术已较为完善,但药物研发往往需要对糖环多个位点进行差异化修饰,以构建具有三维结构多样性的分子库,从而筛选出更高活性的候选药物。现有糖烯双碳官能化技术的瓶颈在于,它既难以实现差异化碳基官能团(如烷基与芳基)的同步引入,更在于无法对最终产物的立体构型进行精准构筑。针对这一难题,该团队提出了双重立体控制反应机制的解决方案:通过糖烯C3位取代基的“空间导向”作用,以及自由基Smiles重排过程中的顺式稠合双环过渡态,反应可高效生成1,2-顺式、2,3-反式构型的产物。以葡萄糖烯为模型底物时,目标产物2-C-支链芳苷的产率达84%,且仅生成α-构型(dr > 19:1),解决了传统反应“立体混乱”的难题。
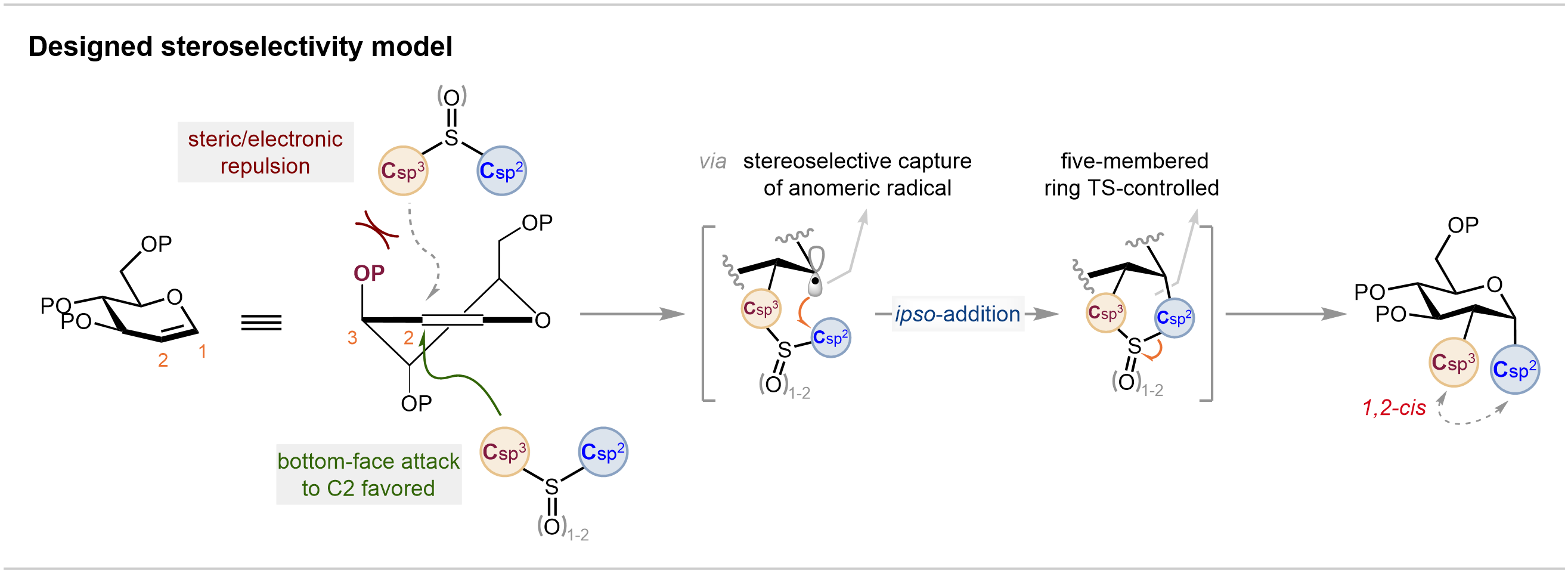
图2. 双重立体控制机制模型
通过该策略,作者成功实现了对不同保护基烯糖的精准C-烷芳基化,制备了一系列结构多样性的2-C-支链芳苷。从单糖(葡萄糖、半乳糖等)到二糖(纤维二糖、乳糖等)衍生的糖烯,均能高效参与反应,甚至含游离羟基的糖烯(无需任何保护)也能转化为目标产物,省去了繁琐的保护基操作。此外,反应还兼容卤素、酮基、酰胺基、膦酸酯基等多种官能团,可轻松引入糖、氨基酸、肽等复杂结构片段,芳基范围也涵盖苯环(含不同取代基)、吡啶、嘧啶、噻吩等,为构建多样化糖衍生物库提供了充足原料。
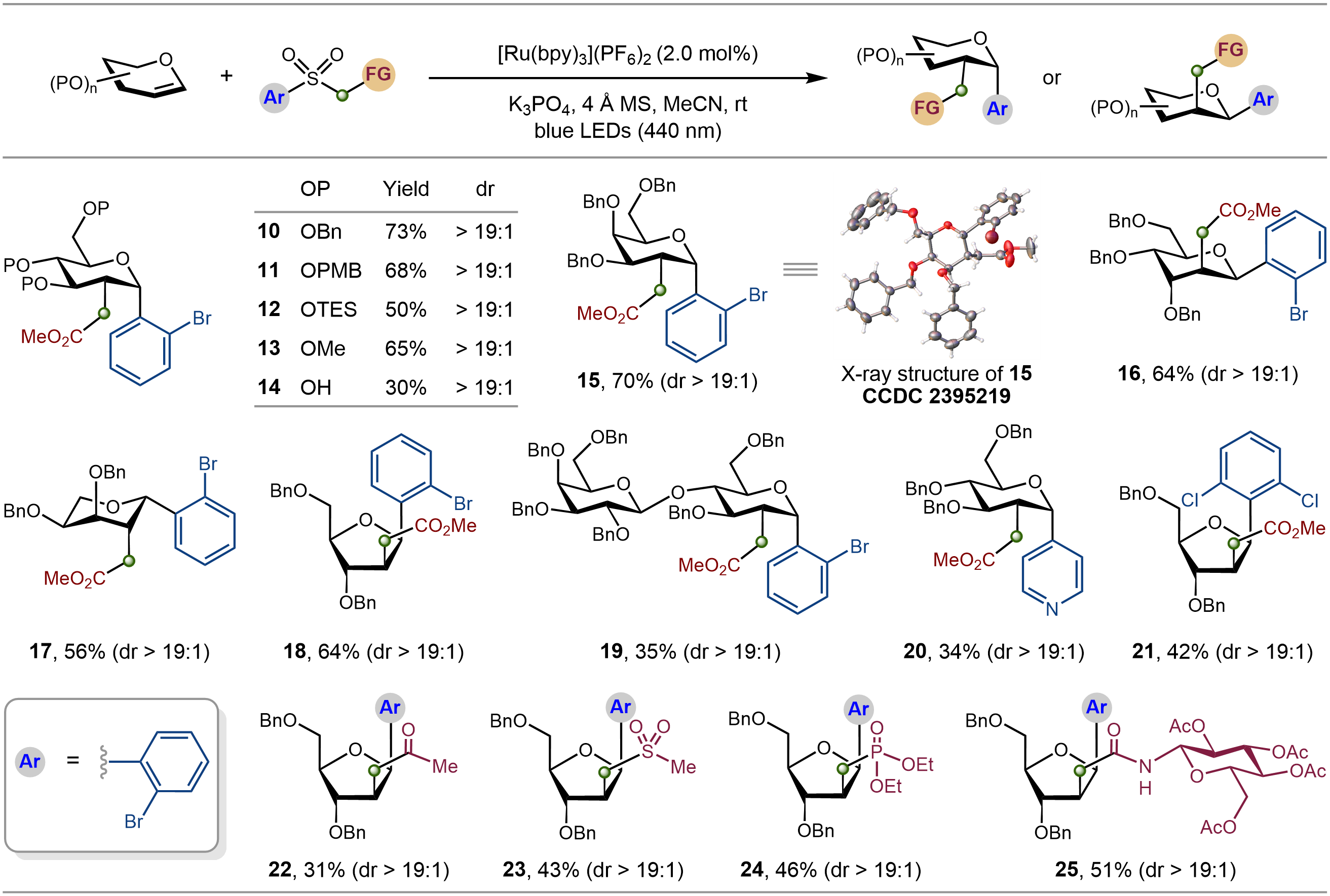
图3. 底物拓展
为验证该方法的实用价值,该团队开展了系统的“下游衍生化”与“生物活性评估”。初步生物活性测试显示,合成的2-C-烷基膦酸酯芳苷表现出优异的抗肿瘤潜力。
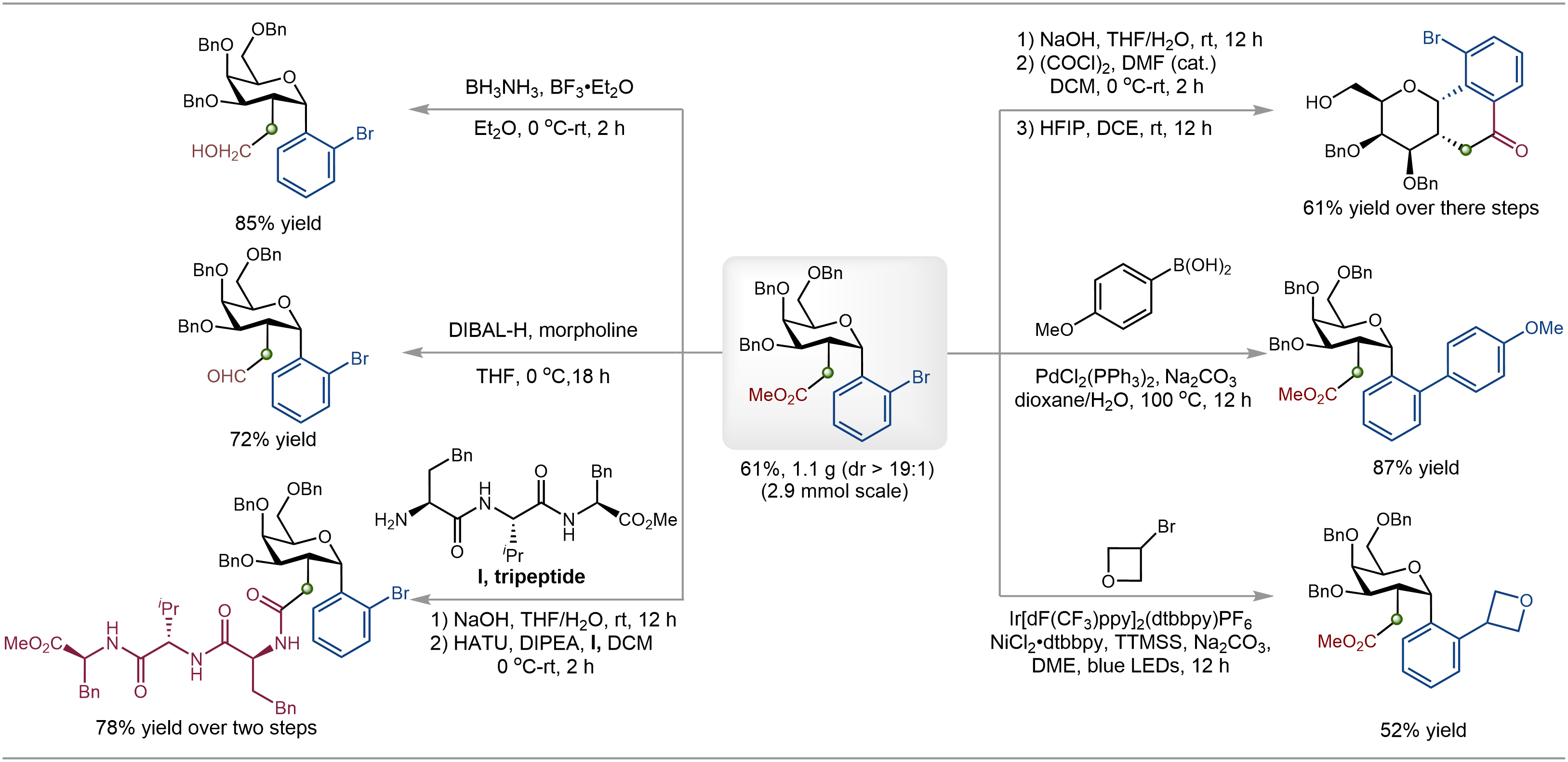
图4. 合成转化
马小锋研究员团队创新性地将光氧化还原催化与自由基Smiles重排相结合,开发出一种糖烯区域和立体选择性1,2-烷芳基化反应,成功实现了糖环双位点的精准同步碳官能团化修饰,构建了一个“模块化、灵活”的糖多样化平台,既解决了“如何精准修饰”的科学问题,又满足了“可放大”的应用需求。该成果以“Streamlined Sugar Diversification via Photoredox-Catalyzed Regio- and Stereoselective 1,2-Alkylarylation of Glycals”为题,发表在国际化学顶级期刊Angew. Chem. Int. Ed.上(影响因子17),成都生物所杨建博士和谢德盟青年副研究员为文章共同第一作者,马小锋研究员为该论文通讯作者。




