人类多功能干细胞高效分化运动神经元及Islet-1的功能
来源:《Nature Communications》
作者:Qiuhao Qu等
时间:2014-03-31
来自囊胚期胚胎的人类胚胎干细胞(hESCs)及从小鼠和人类体细胞诱导多功能干细胞(iPSCs) 后代都为科学进步、生物医学研究和药物开发提供了前所未有的机遇。
运动神经元(MNs)是位于脊髓的一个特殊神经元类别,其轴突以有条理的离散模式指令控制肌肉的活动。它们因脊髓性肌萎缩和侧索硬化等疾病而受到损坏。已经开发了几种从人类胚胎干细胞(hESCs)和人类体细胞诱导多功能干细胞(hiPSCs)分化MNs的方法,但这些程序仍然具有诸如分化程序繁琐、费时(2个月)、需要遗传操作和反复的病毒感染以及低效低产等局限性。此外,分化培养基中含有不确定性因素、动物细胞或动物产品,因此临床不兼容。从人类多能干细胞快速高效高产诱导MNs的发育条件是神经元发育研究、药物筛选和细胞替代疗法的基本要素。
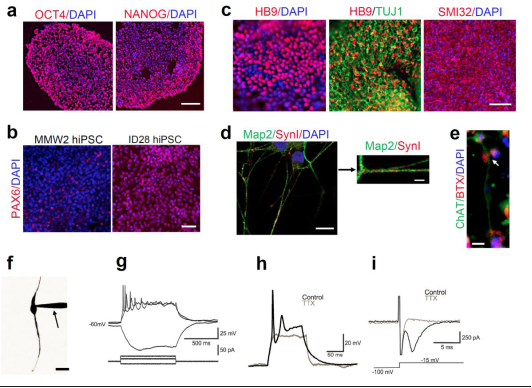
中美研究人员在前期的高效神经诱导基础上,通过严格控制神经形成的时制和全面优化供神经元成长的细胞外基质(ECM)及培养条件,开发了一种快速 (~20天)、高效(约70 %)高产(>250%)的从hESCs和hiPSCs诱导培育成熟及功能化MNs的化学定义贴壁培养方法。该研究显著提高MN的培育条件,这将有助于人类MNs在治疗中的应用。
有趣的是,研究人员发现了人类多功能干细胞诱导形成运动神经元的命运规范:在神经分化初始阶段(第3天),需要苯丙酸去甲睾丸酮化学抑制剂化合物C和BMP 信号等神经形成诱导因素存在。这些调查结果指出一个原生神经先驱群体,其可以采用早期和晚期命运,并且其在人类神经规范过程比以前公认的发生时间更早。
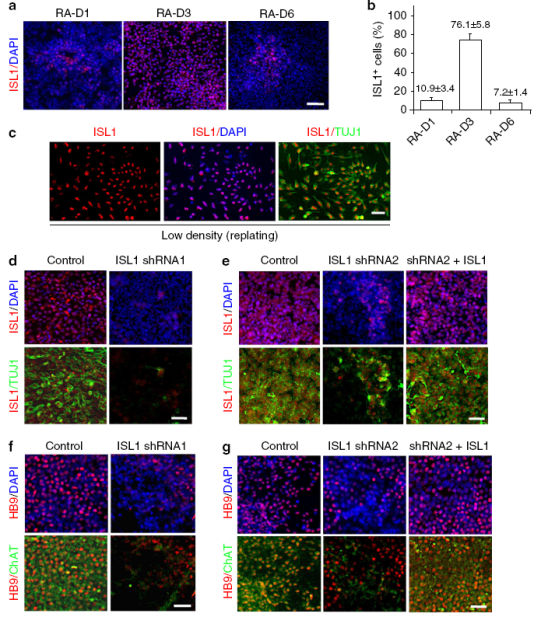
研究人员应用该方法于人类运动神经元发育的分子解剖机制,首次证明胰岛素基因增强结合蛋白-1(ISL1)是由人类胚胎干细胞培育形成成熟及功能化人类MNs所必需的。有趣的是,不像老鼠ISL1删除或减少将导致MNs损失并转换到V2a中间神经元命运,人类ISL1损耗并不会引起细胞死亡或V2a中间神经元转换,这意味着人类和啮齿类动物之间的MN发育具有不同的调节机制。该项研究的发现改进了MN分化策略,推进了对人类神经规范和MN发育的理解,并为人类发展研究、药物研发和再生医学提供了宝贵的工具。(编译:中国科学院成都生物研究所 王芋华,王海燕)
High-efficiency motor neuron differentiation from human pluripotent stem cells
and the function of Islet-1
Abstract Efficient derivation of large-scale motor neurons (MNs) from human pluripotent stem cells is central to the understanding of MN development, modelling of MN disorders in vitro and development of cell-replacement therapies. Here we develop a method for rapid (20 days) and highly efficient (~70%) differentiation of mature and functional MNs from human pluripotent stem cells by tightly modulating neural patterning temporally at a previously undefined primitive neural progenitor stage. This method also allows high-yield (>250%) MN production in chemically defined adherent cultures. Furthermore, we show that Islet-1 is essential for formation of mature and functional human MNs, but, unlike its mouse counterpart, does not regulate cell survival or suppress the V2a interneuron fate. Together, our discoveries improve the strategy for MN derivation, advance our understanding of human neural specification and MN development, and provide invaluable tools for human developmental studies, drug discovery and regenerative medicine.
原文链接:http://www.nature.com/ncomms/2014/140313/ncomms4449/full/ncomms4449.html




